Différenciation de cellules iPSC humaines en corps embryoïdes
L’embryogenèse précoce se caractérise par une succession finement régulée de restrictions de lignage aboutissant à la formation des trois feuillets embryonnaires primaires. Les cellules souches pluripotentes induites (iPSC) constituent un modèle in vitro puissant permettant de reproduire ces événements.
Lorsqu’elles sont agrégées en structures tridimensionnelles appelées corps embryoïdes (Embryoid Bodies, EB), les iPSC se différencient spontanément et donnent naissance à des dérivés ectodermiques, mésodermiques et endodermiques.
Les EB représentent ainsi un modèle largement utilisé pour étudier la différenciation des cellules pluripotentes et les mécanismes précoces du développement. Cependant, leur culture prolongée nécessite des changements fréquents de milieu et une manipulation soigneuse, ce qui peut introduire de la variabilité expérimentale.
L’automatisation étant particulièrement pertinente pour les cellules sensibles, et les corps embryoïdes représentant un modèle de culture à la fois délicat et largement utilisé, nous avons évalué la capacité de Nestor, le système automatisé de culture cellulaire développé par Cellaven, à maintenir et automatiser la différenciation de corps embryoïdes dérivés d’iPSC humaines.
Culture automatisée de corps embryoïdes avec Nestor

Nestor a assuré la culture autonome des cellules iPSC (SCTi003-A, Stemcell Technologies) pendant deux passages. Comme illustré en Figure 1, une fois les cellules prêtes, nous les avons ensemencées manuellement dans des plaques 96 puits à fond en U à faible adhérence, puis cultivées sous forme de sphéroïdes auto-agrégés pendant trois jours dans du milieu eTeSR complété avec de la blébbistatine (1:2000) (Stemcell Technologies).
Une fois les sphéroïdes pleinement formés, ceux-ci ont été transférés dans des plaques 24 puits adhérentes préalablement revêtues de Matrigel, puis alimentés quotidiennement avec du milieu hESC frais par Nestor.
Pendant 21 jours consécutifs, Nestor a permis une culture continue sans intervention durant les week-ends.
Différenciation des corps embryoïdes évaluée par l’analyse morphologique et les marqueurs des feuillets embryonnaires

Les EB en cours de différenciation ont été observés quotidiennement en microscopie en champ afin de contrôler l’adhérence à la matrice et l’étalement cellulaire.
Comme illustré en Figure 2, au jour 1, les EB présentaient un diamètre compris entre 745 et 920 µm (à droite). À partir du jour 7 (au centre), les cellules ont commencé à migrer et à s’étaler à partir du sphéroïde initial, pour finalement former, au jour 20 (à gauche), des structures matures et organisées présentant des motifs caractéristiques du développement embryonnaire.
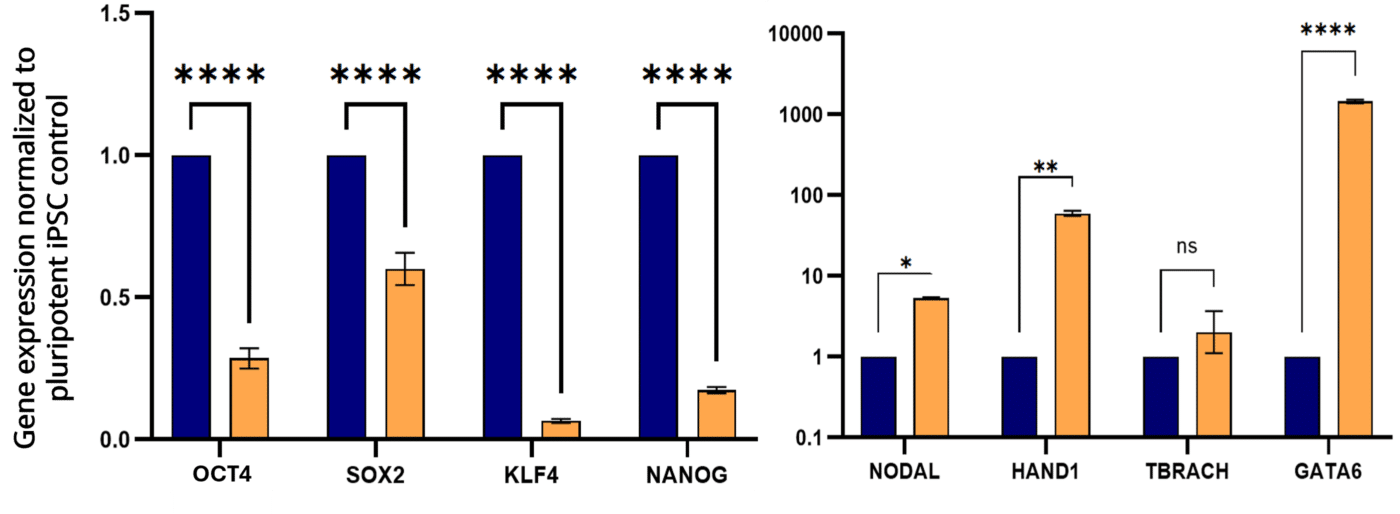
Au jour 21, une analyse RT-qPCR a été réalisée afin d’évaluer les modifications du profil d’expression génique des EB par rapport aux iPSC non différenciées.
Comme illustré en Figure 3, les EB présentent une diminution significative de l’expression des marqueurs de pluripotence (ANOVA à deux facteurs, p < 0,001, n = 3).
En revanche, l’analyse des gènes spécifiques des feuillets embryonnaires indique une différenciation nette des EB comparativement aux iPSC contrôle. Les EB âgés de 21 jours expriment des gènes associés aux trois feuillets embryonnaires.
Les gènes NODAL et HAND1 (mésoderme), ainsi que GATA6 (endoderme), présentent une augmentation significative de leur expression dans les EB.
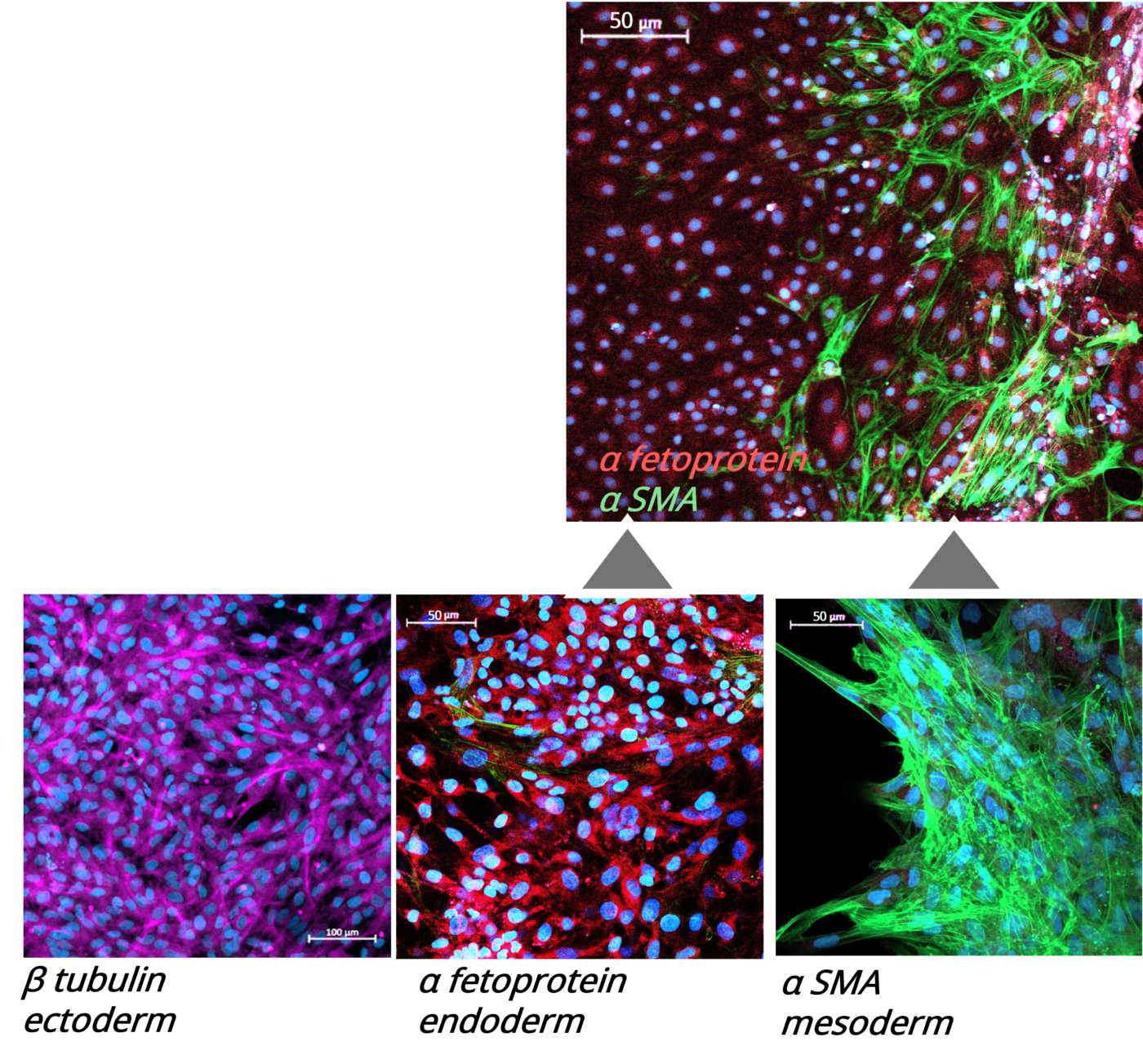
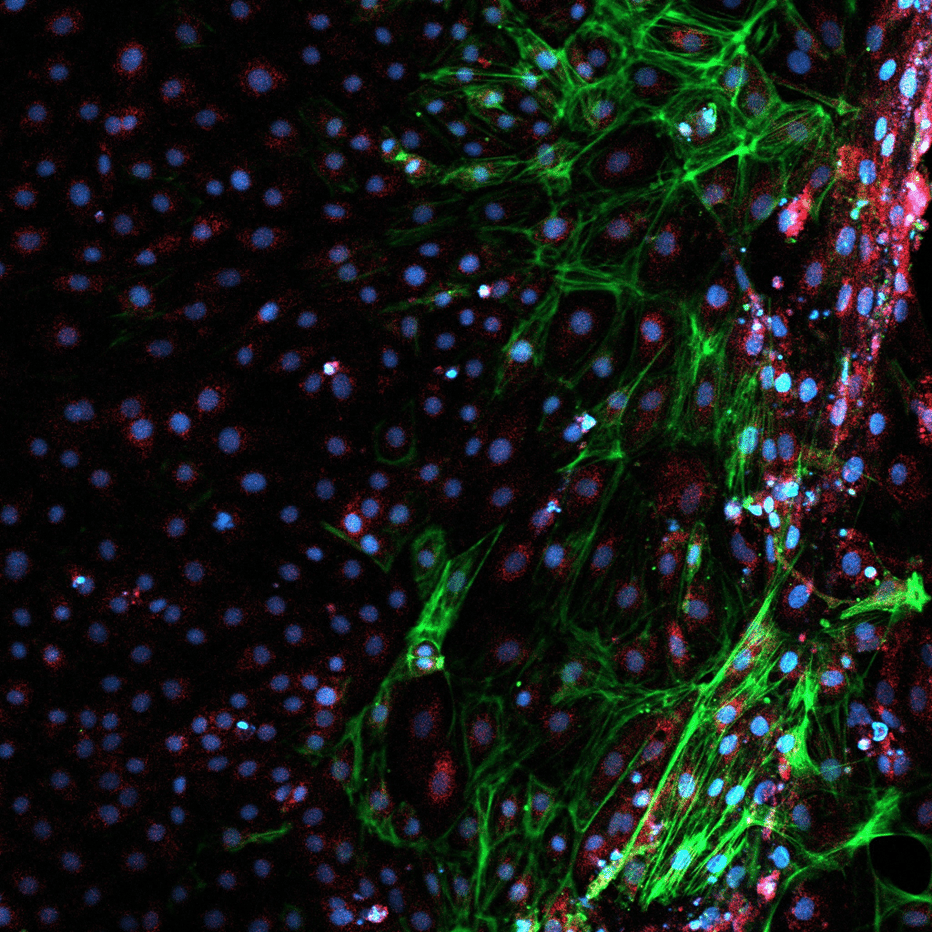
Afin d’évaluer si les modifications du profil d’expression génique se traduisaient par une production protéique correspondante, nous avons réalisé un marquage immunofluorescent des EB à l’aide d’anticorps dirigés contre des marqueurs spécifiques des trois feuillets embryonnaires : α-fœtoprotéine humaine (souris, BioLegend), α-SMA humaine (lapin, Abcam) et β-tubuline III humaine (souris, BioLegend).
En raison d’une réactivité croisée entre certains anticorps, les marquages de l’endoderme et de l’ectoderme ont été réalisés séparément.
Comme illustré en Figure 4, les EB âgés de 21 jours expriment des protéines caractéristiques des trois feuillets embryonnaires.
Différenciation stable de corps embryoïdes issus de cellules iPSC humaines avec Nestor
Cette étude démontre la capacité de Nestor à assurer une différenciation prolongée de corps embryoïdes. L’automatisation n’a pas altéré le potentiel des iPSC à se différencier spontanément en dérivés des trois feuillets embryonnaires.
Le système d’aspiration douce intégré au couvercle de plaque n’a pas perturbé la morphologie ni l’adhérence des corps embryoïdes.
Un environnement de culture stable a permis aux sphéroïdes dérivés d’iPSC de perdre progressivement leur pluripotence et d’exprimer des gènes associés aux différents feuillets embryonnaires.
D’un point de vue fonctionnel, les corps embryoïdes différenciés automatiquement expriment également des protéines clés de manière régionale. Cette organisation spatiale caractéristique suggère une différenciation spontanée efficace et des interactions fonctionnelles entre les cellules et leur microenvironnement
Références
- Pineda ET et al. Differentiation patterns of embryonic stem cellsin two– versus three-dimensional culture. CellsTissues Organs. 2013 Feb
- Manuela Jaklinet al. Focus on germ-layer markers: A humanstem cell-basedmodel for in vitro teratogenicitytesting, Reproductive Toxicology, 2020.
Auteurs
Duncan Alric, Houda Djedaini, Harald Chaboud, Alexandre Houzé, Lisa Morisseau, Julien Maruotti
07/2025. Cellaven, Besançon, France